
姓名:
朱金根
职称:
教授 博士生导师 硕士生导师
性别:
男
毕业院校:
兰州大学
学位:
博士
在职信息:
在职
所在单位:
生物工程学院
学科:
生物学 生物医药 生物工程
办公地点:
大连理工大学生物工程学院411
电子邮箱:
zhujingen@dlut.edu.cn
团队聚焦噬菌体及腺相关病毒(AAV)载体工程及其在基因治疗和疫苗开发领域的研究。基因和细胞治疗作为生物医药领域的前沿方向,近年来发展迅速,已有多款药物获批上市。然而,现有主流病毒递送载体在基因包装容量(AAV <4.7 kb)、生产成本和安全性等方面仍存在显著瓶颈。团队基于噬菌体超大基因组容量、生产成本低、结构稳定、安全性高等优势,通过工程化改造和模块化组装,创建具备大容量基因和蛋白质递送能力的“人工病毒载体”平台,突破长片段基因递送瓶颈;同时建立多联多价噬菌体黏膜疫苗平台,应用于呼吸道病毒(流感、新冠等)和肿瘤疫苗开发,并推动成果转化。
主要研究方向:(1) 噬菌体“人工病毒载体”工程化改造与大容量基因递送;(2) 腺相关病毒(AAV)载体工程及应用;(3) 多联多价噬菌体黏膜疫苗研发与免疫机制研究;(4) 天然噬菌体资源发掘与RNA/DNA噬菌体载体平台开发
1. 创建基于噬菌体和AAV的“人工病毒载体”平台,突破长片段基因递送瓶颈
提出“衣壳载体”概念,系统构建了从空衣壳制备、DNA装载、功能化修饰、模块化组装到哺乳动物细胞递送的全流程体系。建立“ATP驱动-非序列依赖性DNA包装反应体系”,可在数分钟内完成高达171 kb的任意治疗DNA装载。构建“超酸性T4衣壳”、“细胞核引导转运系统”和噬菌体-AAV杂合载体,显著提升了细胞内涵体逃逸能力及长片段基因的细胞核递送效率。成功递送了全长肌营养不良蛋白Dystrophin基因(约11 kb)。该成果以第一作者发表于Nature Communications(2023,2026)和Science Advances(2019),被GEN等10余家国际媒体专题报道。
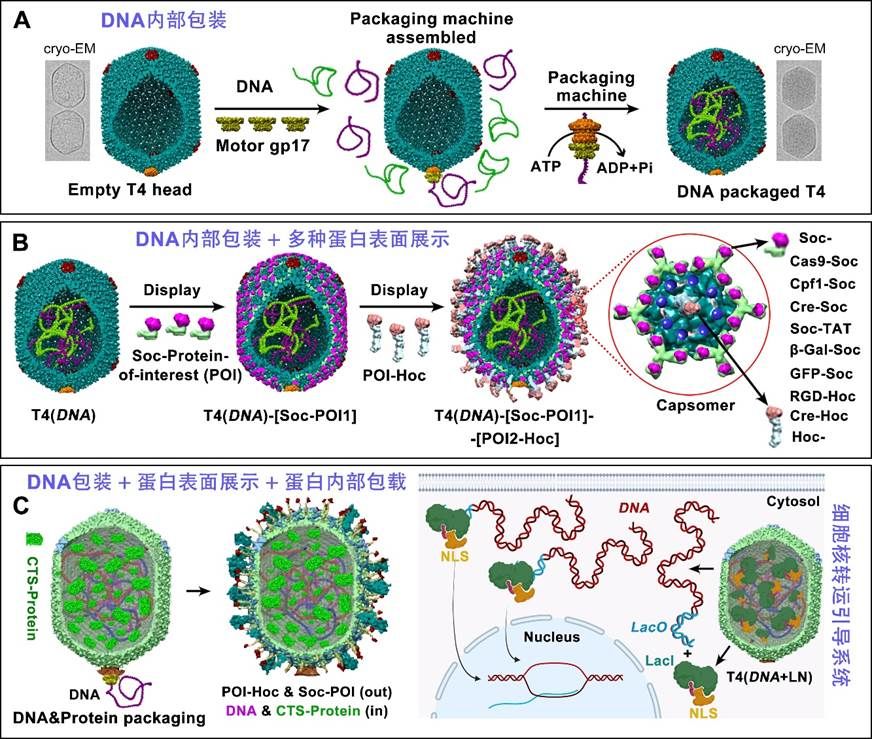
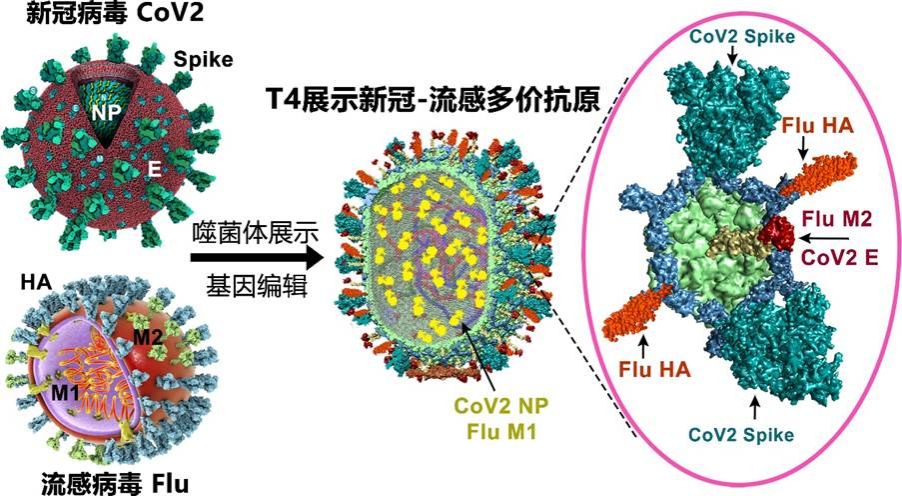
2. 创建多联多价噬菌体黏膜疫苗平台,实现黏膜免疫强效激活
创建“CRISPR-Cas程序化空间释放与长片段精准插入”技术,将同源重组效率从传统的10⁻⁵–10⁻⁴提升至1%–10%。建立“噬菌体展示+包装”多抗原整合策略,成功实现了新冠和流感病毒六种关键抗原在单个T4上的组合展示。鼻内免疫的T4疫苗对新冠原始株、变异株及流感病毒均提供了完全保护,中和抗体水平比肌肉注射疫苗高3倍。美国微生物学会旗舰期刊mBio将其选为亮点报道。该技术已获三项专利并授权企业转化生产(Science Advances, 2021; mBio, 2022; Annual Review of Virology, 2024; Small Science, 2025)。
围绕T4噬菌体及AAV,共获得5项国际授权专利,涵盖噬菌体衣壳载体构建、杂合病毒载体组装、CRISPR噬菌体编辑及黏膜疫苗设计等核心技术 (US20230355738A1; US20220184205A1; US20220090139A1; US20210054410A1; US Application No. 63/698,596)。
代表论文:
(1) Zhu J, Batra H, Ananthaswamy N, Mahalingam M, Tao P, Wu X, Guo W, Fokine A, Rao VB. Design of bacteriophage T4-based artificial viral vectors for human genome remodeling. Nature Communications, 2023, 14: 2928
(2) Zhu J, Ananthaswamy N, Jain S, et al. A universal bacteriophage T4 nanoparticle platform to design multiplex SARS-CoV-2 vaccine candidates by CRISPR engineering. Science Advances, 2021, 7: eabh1547
(3) Zhu J, Tao P, Mahalingam M, et al. A prokaryotic-eukaryotic hybrid viral vector for delivery of large cargos of genes and proteins into human cells. Science Advances, 2019, 5: eaax0064
(4) Han L#, Mao Q#, Zhu J#, Jin X, et al. Cryo-EM structures of bacteriophage T4 portal-neck connector complexes reveal a viral genome retention mechanism involving a host component. Nature Communications, 2026, 17, 1964 (#共同第一作者)
(5) Fokine A*, Zhu J, Klose T, Vago F, et al. In situ atomic structures of the portal-neck-tail complex of bacteriophage T4 inform a viral genome positioning mechanism. Nature Communications, 2026, 17, 1965
(6) Zhu J*, Sha J, Batra H, et al. A modular bacteriophage T4 nanoparticle platform enables rapid design of dual COVID-19-Flu mucosal vaccines. Small Science,2025, 5(4): 2400580(第一作者兼共同通讯)
(7) Zhu J*, Tao P, Chopra AK, Rao VB*. Bacteriophage T4 as a Protein-Based, Adjuvant-and Needle-Free, Mucosal Pandemic Vaccine Design Platform. Annual Review of Virology,2024, 11(1):395-420(第一作者兼共同通讯)
(8) Zhu J #, Jain S #, Sha J #, Batra H, et al. A bacteriophage-based, highly efficacious, needle and adjuvant-free, mucosal COVID-19 vaccine. mBio,2022,13(4):e0182222(#共同第一作者,Editor’s Pick)
朱金根 博士 教授
办公地点:大连理工大学生物工程学院411室
E-mail: zhujingen@dlut.edu.cn